Luyện tập. Một hợp chất hữu cơ Y có 32% C, 6,67% H, 18,67% N về khối lượng còn lại là O. Phân tử...
Câu hỏi:
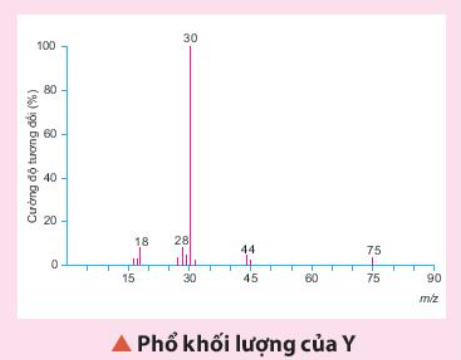
Luyện tập. Một hợp chất hữu cơ Y có 32% C, 6,67% H, 18,67% N về khối lượng còn lại là O. Phân tử khối của hợp chất này được xác định thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất. Lập công thức phân tử của Y
Câu trả lời:
Người trả lời: GV. Đỗ Văn Hạnh
Để giải bài toán trên, ta cần sử dụng phương pháp giải hợp chất hữu cơ. Đầu tiên, ta tính phần trăm khối lượng của từng nguyên tố trong hợp chất Y:%C = 32%H = 6.67%N = 18.67Ta tiến hành chuyển đổi phần trăm thành số mol:m(C) = 32gm(H) = 6.67gm(N) = 18.67gn(C) = m(C)/12n(H) = m(H)/1n(N) = m(N)/14Tiếp theo, ta tính phần trăm khối lượng O:%C + %H + %N + %O = 10032 + 6.67 + 18.67 + %O = 100%O = 42.66Do đó, ta có:m(O) = 42.66n(O) = m(O)/16Sau đó, ta tính tổng số mol trong hợp chất Y:n = n(C) + n(H) + n(N) + n(O)Cuối cùng, ta xác định công thức phân tử của Y thông qua kết quả phổ khối lượng với peak ion phân tử có giá trị m/z lớn nhất.Trả lời câu hỏi: Công thức phân tử của hợp chất Y có thể được xác định dựa trên các phần trăm khối lượng của các nguyên tố trong hợp chất và thông qua phổ khối lượng để xác định peak ion phân tử có giá trị m/z lớn nhất. Để xác định công thức phân tử chính xác, ta cần tính toán số mol của từng nguyên tố và tổng số mol trong hợp chất sau đó tìm ra phần tử cần thiết để hoàn thiện công thức phân tử.
Câu hỏi liên quan:
- MỞ ĐẦUPhổ khối lượng (Mass spectrometry - MS) thường được sử dụng để xác định nguyên tử khối, phân...
- 1. XÁC ĐỊNH PHÂN TỬ KHỐI CỦA HỢP CHẤT HỮU CƠSử dụng kết quả phổ khối lượng để xác định phân tử khối...
- 2. CÔNG THỨC PHÂN TỬ HỢP CHẤT HỮU CƠLập công thức phân tử hợp chất hữu cơ từ dữ liệu phân tích...
- BÀI TẬPBài tập 1. Acetone là một hợp chất hữu cơ dùng để làm sạch dụng cụ trong phòng thí nghiệm,...
- Bài tập 2. Chất hữu cơ X được sử dụng khá rộng rãi trong ngành y tế với tác dụng chống vi khuẩn, vi...
- Bài tập 3. Aniline là hợp chất quan trọng trong công nghiệp phẩm nhuộm sản xuất polymer. Kết quả...
Bình luận (0)




