14.5. Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết (Bảng 14.1 sách giáo khoa...
Câu hỏi:
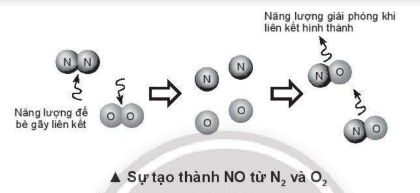
14.5. Tính nhiệt tạo thành chuẩn của HF và NO dựa vào năng lượng liên kết (Bảng 14.1 sách giáo khoa (SGK)), của F2 H2, HF, N2, O2, NO. Giải thích sự khác nhau về nhiệt tạo thành của HF và NO.
Câu trả lời:
Người trả lời: GV. Đỗ Đăng Việt
Phương pháp giải:1. Xác định năng lượng liên kết của nguyên tử trong phân tử theo Bảng 14.1 trong sách giáo khoa.2. Sử dụng công thức $\Delta _{r}H_{298}^{o}=\sum E_{b}(cđ) - \sum E_{b}(sp)$ để tính nhiệt tạo thành chuẩn của HF và NO.3. So sánh nhiệt tạo thành của HF và NO để giải thích sự khác nhau.Câu trả lời cho câu hỏi trên:Nhiệt tạo thành chuẩn của HF là -539 kJ/mol, trong khi đó nhiệt tạo thành chuẩn của NO là +181 kJ/mol. Sự khác nhau này xuất phát từ khả năng tạo liên kết của nguyên tử trong phân tử. Trong HF, nguyên tử H và F tạo liên kết cường độ cao do sự chênh lệch lớn về điện âm giữa hai nguyên tử, dẫn đến năng lượng liên kết lớn và nhiệt tạo thành âm. Trong khi đó, trong NO, nguyên tử N và O tạo liên kết không mạnh bằng do chênh lệch về điện âm không lớn, dẫn đến năng lượng liên kết nhỏ và nhiệt tạo thành dương. Điều này làm cho phản ứng tạo thành NO không xảy ra ở điều kiện thường mà cần điều kiện năng lượng cao hơn.
Câu hỏi liên quan:
- 14.1. Cách tính enthalpy của phản ứng hoá học dựa vào năng lượng liên kết và enthalpy tạo thành của...
- 14.2. Cho phản ứng tổng quát : aA + bB→mM + nN . Hãy chọn các phương án...
- 14.3. Thành phần chính của đa số các loại đá dùng trong xây dựng là CaCO3, chúng vừa có tác dụng...
- 14.4. Propene là nguyên liệu cho sản xuất nhựa polypropylene (PP). PP được sử dụng để sản xuất các...
- 14.6. Phosgene là chất khí không màu, mùi cỏ mục, dễ hoá lỏng; khối lượng riêng 1,420 g/cm$^{3}$ (ở...
- 14.7. Kim loại nhôm có thể khử được oxide của nhiều nguyên tố. Dựa vào nhiệt tạo thành chuẩn của...
- 14.8*. Cho 3 hydrocarbon X, Y, Z đều có 2 nguyên tử C trong phân tử. Số nguyên tử H trong các phân...
- 14.9. Cho các phản ứng:CaCO3 (s) → CaO (s) + CO2(g) $\Delta _{r}H_{298}^{o}$= + 178,49 kJC2H5OH (l)...
- 14.10. Lactic acid hay acid sữa là hợp chất hoá học đóng vai trò quan trọng trong nhiều quá trình...
- 14.11. Chloromethane (CH3CI), còn được gọi là methyl chloride, Refrigerant – 40 hoặc HCC 40. CH3Cl...
- 14.12*. Một xe tải đang vận chuyển đất đèn (thành phần chính là CaC2 và CaO) gặp mưa xảy ra sự cố,...
- 14.13. Cho phương trình hoá học của phản ứng:C2H2 (g) + H₂O (l) → C2H5OH (I)Tính biến thiên...
- 14.14*. Cho phản ứng phân huỷ hydrazine: N2H4(g)→N2(g) + 2H2(g)a) Tính $\Delta...
- 14.15. Quá trình hoà tan calcium chloride trong nước:CaCl2 (s) → Ca2+ (aq) + 2Cl-...
Bình luận (0)




